Un peptide è a molecola composto da due o più aminoacidi collegati tra loro da legami peptidici. La struttura generale di un amminoacido è: R-CH (NH2) COOH. Ogni aminoacido è a monomero che forma una catena polimerica peptidica con altri aminoacidi quando il gruppo carbossilico (-COOH) di un amminoacido reagisce con il gruppo amminico (-NH2) di un altro amminoacido, formando a legame covalente tra i residui di amminoacidi e il rilascio di una molecola di acqua.
Key Takeaways: peptidi
- Un peptide è un polimero formato collegando le subunità aminoacidiche.
- Una molecola di peptide può essere biologicamente attiva da sola o può agire come una subunità per una molecola più grande.
- Le proteine sono essenzialmente peptidi molto grandi, spesso costituiti da più subunità peptidiche.
- I peptidi sono importanti in biologia, chimica e medicina perché sono elementi costitutivi di ormoni, tossine, proteine, enzimi, cellule e tessuti corporei.
funzioni
I peptidi sono molecole importanti dal punto di vista biologico e medico. Si verificano naturalmente all'interno degli organismi, più i composti sintetizzati in laboratorio sono attivi quando introdotti in un corpo. I peptidi agiscono come componenti strutturali di cellule e tessuti, ormoni, tossine, antibiotici ed enzimi. Esempi di peptidi includono l'ormone ossitocina, il glutatione (stimola la crescita dei tessuti), la melittina (veleno d'api del miele), l'insulina dell'ormone pancreatico e il glucagone (un fattore iperglicemico).
Sintesi
Ribosomi nelle cellule costruire molti peptidi, poiché l'RNA viene tradotto in una sequenza di amminoacidi e i residui sono collegati tra loro. Esistono anche peptidi nonribosomici, che sono costruiti da enzimi piuttosto che da ribosomi. In entrambi i casi, una volta che gli aminoacidi sono stati collegati, subiscono modifiche post-traduzionali. Questi possono includere idrossilazione, solfonazione, glicosilazione e fosforilazione. Mentre la maggior parte dei peptidi sono molecole lineari, alcuni formano anelli o strutture lariatiche. Meno spesso, gli amminoacidi L subiscono la racemizzazione per formare amminoacidi D all'interno dei peptidi.
Peptide contro proteine
I termini "peptide" e "proteina" sono comunemente confusi. Non tutti i peptidi formano proteine, ma tutte le proteine sono costituite da peptidi. Le proteine sono grandi peptidi (polipeptidi) contenenti 50 o più aminoacidi o molecole costituiti da più subunità peptidiche. Inoltre, le proteine in genere ne visualizzano di più struttura complessa rispetto ai peptidi più semplici.
Classi di peptidi
I peptidi possono essere classificati in base alla loro funzione o alla loro fonte. Il Manuale dei peptidi biologicamente attivi elenca gruppi di peptidi, tra cui:
- Peptidi antibiotici
- Peptidi batterici
- Peptidi cerebrali
- Peptidi antitumorali e antitumorali
- Peptidi cardiovascolari
- Peptidi endocrini
- Peptidi fungini
- Peptidi gastrointestinali
- Peptidi invertebrati
- Peptidi di oppiacei
- Peptidi vegetali
- Peptidi renali
- Peptidi respiratori
- Peptidi vaccinali
- Peptidi velenosi
Nomina dei peptidi
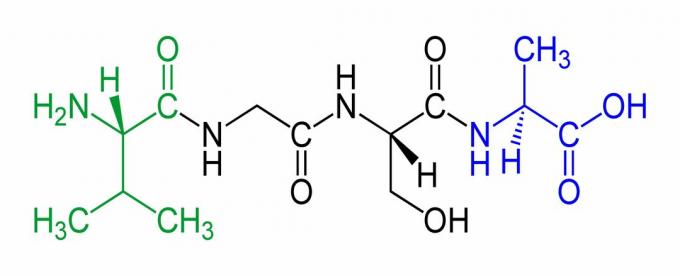
I peptidi sono nominati in base a quanti residui di aminoacidi contengono o in base alla loro funzione:
- Monopeptide: costituito da un aminoacido
- Dipeptide: composto da due aminoacidi
- Tripeptide: ha tre aminoacidi
- Tetrapeptide: ha quattro aminoacidi
- Pentapeptide: ha cinque aminoacidi
- Esapeptide: ha sei aminoacidi
- Eptapeptide: ha sette aminoacidi
- Octapeptide: ha otto aminoacidi
- Nonapeptide: ha nove aminoacidi
- Decapeptide: contiene dieci aminoacidi
- Oligopeptide: composto da due a venti aminoacidi
- Polipeptide: catena lineare di molti aminoacidi collegati da legami ammidici o peptidici
- Proteine: sono composte da più di 50 aminoacidi o più polipeptidi
- Lipopeptide: consiste in un peptide legato a un lipide
- Neuropeptide: qualsiasi peptide attivo nel tessuto neurale
- Agente peptidergico: sostanza chimica che modula il funzionamento dei peptidi
- Proteose: peptidi prodotti dall'idrolisi delle proteine
Peptidi nello sport
Due tipi di peptidi sono classificati come sostanze vietate nell'Allegato 2 (S2) sulla World Anti-Doping Agency (WADA) Elenco vietato, Elenco vietato dell'Agenzia antidoping degli Stati Uniti (USADA) e dall'Australian Sports Anti-Doping Autorità. Gli ormoni peptidici e i peptidi secretagoghi sono vietati per l'uso da parte di atleti professionisti, indipendentemente dal fatto che siano in competizione, perché le sostanze chimiche agiscono come esaltatori di prestazioni. I peptidi vietati sono gli ormoni della crescita, quelli che aumentano l'ossigenazione del sangue, quelli che colpiscono i muscoli crescita e riparazione e quelli che causano la secrezione di organi del sistema endocrino (ad es. ovaie, testicoli, tiroide) ormoni. Le sostanze sono vietate non solo perché possono dare agli atleti un vantaggio sleale rispetto ai coetanei, ma perché il loro uso può aumentare il rischio di ipertensione, intossicazione da acqua, danni al cuore e al fegato e cancro.
fonti
- Abba J. Kastin, ed. (2013). Manuale di peptidi biologicamente attivi (2a edizione). ISBN 978-0-12-385095-9.
- Ardejani, Maziar S.; Orner, Brendan P. (2013-05-03). "Obbedisci alle Regole dell'Assemblea del Peptide" Scienza. 340 (6132): 561–562. doi:10.1126 / science.1237708
- Finking R, Marahiel MA; Marahiel (2004). "Biosintesi dei peptidi nonribosomici". Revisione annuale di microbiologia. 58 (1): 453–88. doi:10,1146 / annurev.micro.58.030603.123615
- IUPAC. Compendio di terminologia chimica, 2a ed. (il "Libro d'oro"). Compilato da A. D. McNaught e A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). ISBN 0-9678550-9-8.